Hoe worden hartritmestoornissen eigenlijk veroorzaakt? We weten dat er bij PLN hartritmestoornissen optreden en dat PLN calcium reguleert. Calcium is belangrijk voor de omzetting van een elektrisch signaal in de samentrekking van het hart. Het is dus aannemelijk dat deze twee verband met elkaar houden. In dit artikel bespreken we een onderzoek dat heel nauwkeurig heeft gekeken hoe een verstoring van calcium tot ritmestoornissen (aritmie) zou kunnen leiden.
Voor dit onderzoek werden muizenharten gebruikt waar we al eerder over schreven. In het vorige artikel bleek dat er in muizen PLN harten geen veranderingen zijn in structuur, maar dat er wel veranderingen worden gevonden in de elektrische activatie in het hart. Deze veranderingen zijn zowel op molecuulniveau als op bijvoorbeeld een hartfilmpje zichtbaar. Dit artikel bouwt voort op deze bevindingen door te onderzoeken of veranderde elektrische activatie leidt tot hartritmestoornissen.
HET MENSENHART EN HET MUIZENHART
Het bestuderen van hartritmestoornissen in muizen is niet zo makkelijk. Het muizenhart slaat namelijk zo’n 600 keer per minuut! Ons menselijke hart daarentegen trekt ongeveer 70 keer per minuut samen in rust. Interessant is wel dat onze hartslag bij inspanning stijgt tot 120-150 slagen per minuut (een stijging van 70-110%), terwijl een muizenhart niet hoger komt dan 700-800 keer (een stijging van 17-33%). Het menselijk hart is dus veel beter in staat zich aan te passen. Door hun hoge hartslag hebben muizen minder kans op hartritmestoornissen: voordat de minste of geringste afwijking ontstaat, komt er al weer een nieuwe hartslag die alles weer recht trekt.
Uit zichzelf vertonen de PLN harten dan ook geen verstoring van het hartritme. Na stimulatie met een stofje dat op adrenaline lijkt, verandert dit. De PLN harten hebben een grotere kans op ritmestoornissen dan de gezonde harten. Als we inzomen, blijkt met name de rechterkamer afwijkend te zijn. De elektrische activatie gaat daar trager, er zijn meer verschillen in de elektrische activatie en de hartcellen reageren niet goed op adrenaline.
Elektrische activiteit
In deze vervolgstap wordt geavanceerde beeldvorming gebruikt om te kijken hoe de elektrische activiteit zich door het hart verplaatst. Wat blijkt? In het PLN hart ontstaat een soort file (Figuur 1). Het elektrische signaal wordt traag doorgegeven terwijl er ondertussen al een nieuw signaal aankomt. Daarbij komt nog een tweede probleem: in PLN harten zitten plekken met vet- en bindweefsel.
Deze plekken worden slecht geactiveerd door de elektrische signalen waardoor het signaal wordt vertraagd of zelfs geblokkeerd. Op deze plekken kan nog iets gebeuren. Normaal gesproken wordt het signaal in een rechte lijn doorgegeven. Maar doordat er nu een plek is waar het signaal slecht wordt doorgegeven, ontstaat er een spiraal, een soort wervelwind, om dit plekje heen.
Wervelvind in het hart
Zo ontstaat een eilandje van cellen die niet geactiveerd worden. Deze verstoring kan het begin van een ritmestoornis zijn. In gezonde muizenharten komt zo’n wervelwind ook wel eens voor, maar in PLN harten hebben ze een aantal eigenschappen waardoor ze sneller een probleem worden. In de PLN harten kan de wervelwind bij een lagere hartslag ontstaan waardoor ze minder makkelijk hersteld worden. Door de problemen in PLN harten ontstaat er vaker een wervelwind rond regio’s met een vertraagde activatie en in de rechterkamer.
Daarnaast duren de wervelwinden langer en draaien ze sneller rond dan de hartslag waarbij ze ontstaan. Dit hangt met elkaar samen: er zijn problemen met de geleiding in de rechterkamer en doordat de wervelwind sneller ronddraait dan de hartslag is het moeilijker om hem te stoppen. Ten slotte verplaatsen de wervelwinden zich in PLN harten sneller en zijn er afwijkingen in het weefsel die verder gaan dan simpelweg een verhoogde kans op ritmestoornissen.
Deze complexe studie laat een deel van het mechanisme achter hartritmestoornissen bij PLN zien. Hierbij blijkt dat er veranderingen in het hartweefsel zijn die tot ritmestoornissen kunnen leiden voordat er veranderingen in de structuur of werking van het hart zijn. Deze veranderingen kunnen het elektrische signaal blokkeren of een wervelwind veroorzaken die het signaal verstoord. Hiermee ontrafelt deze studie een stukje van het mechanisme achter hartritmestoornissen in PLN.
DE AUTEURS VAN DIT ONDERZOEK
Dit onderzoek werd geleid door Francesca Stilltano en Fadi Akar. Professor Akar is beroemd voor zijn onderzoek naar artimiën. Akar heeft jarenlang in New York gewerkt en is nu verbonden aan de beroemde Yale University. Francesca Stillitano heeft jarenlang in New York gewerkt en is sinds 2022 vanuit Utrecht bijna fulltime bezig met PLN onderzoek. Eerste auteur is Nour Raad. Zij werkt in Duitsland als cardioloog, maar heeft eerder in New York onderzoek gedaan naar PLN.
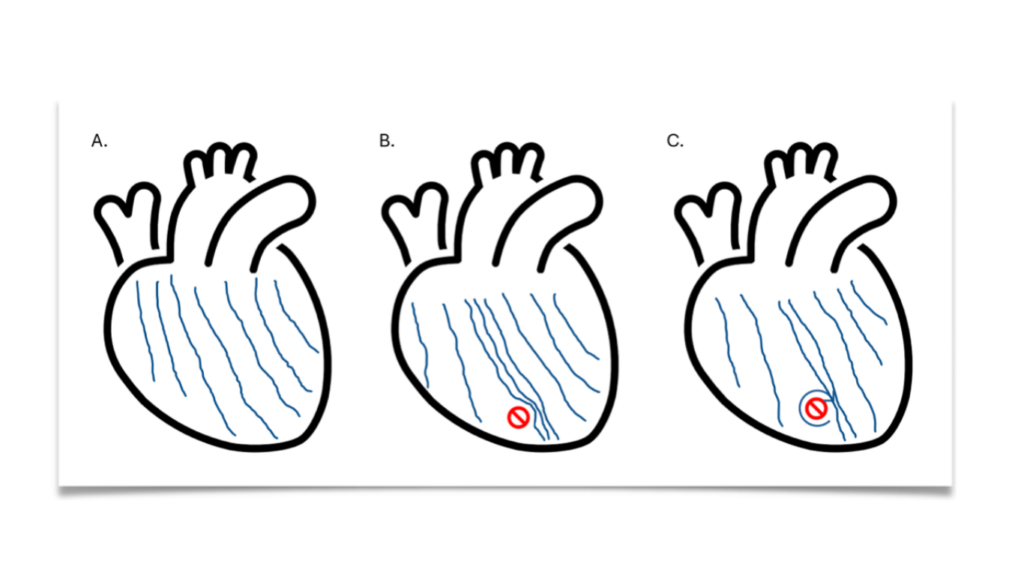
Figuur 1 Tekening van de golven van elektrische activatie. In een gezond hart (A) bewegen de elektrische golven redelijk recht en met gelijke onderlinge afstand. In een PLN hart (B) worden de golven vertraagd op de scheiding van de linker- en rechter harthelft. Hierdoor ontstaat een file. Daarnaast is er vet- en bindweefsel aanwezig (gele plek) waar het signaal niet goed wordt doorgegeven. Om deze plek heen kan een wervelwind ontstaan (C).
Raad, 2021, Circulation Arrhythmia Mechanism and Dynamics in a Humanized Mouse Model of Inherited Cardiomyopathy due to Phospholamban R14del Mutation
