In een eerder artikel hebben we beschreven hoe het PLN-gen in een gezond hart werkt. Mensen met de PLN-R14del ziekte zijn drager van een verandering in dit gen, het zogenaamde PLN-R14del gen. Hierbij mist er een stukje van de DNA code, waardoor het PLN eiwit een ingrediënt mist. Dit is ingrediënt nummer 14, een arginine. Hoe zorgt dit foutje voor het ontstaan van de ziekte?
Op dit moment weten we nog niet precies hoe de ziekte ontstaat. Er zijn twee theorieën (in de biologie betekent dat meestal dat beide een beetje waar zijn). Voor beide bestaat wetenschappelijk bewijs, maar beide vertonen ook gebreken. Oorspronkelijk dacht men dat PLN-R14del de functie van PLN op de calciumhuishouding versterkt. Later zijn er aanwijzingen gevonden dat het PLN-R14del eiwit zelf giftig is. We leggen beide theorieën uit.
Theorie 1: PLN-R14del versterkt de calciumhuishouding
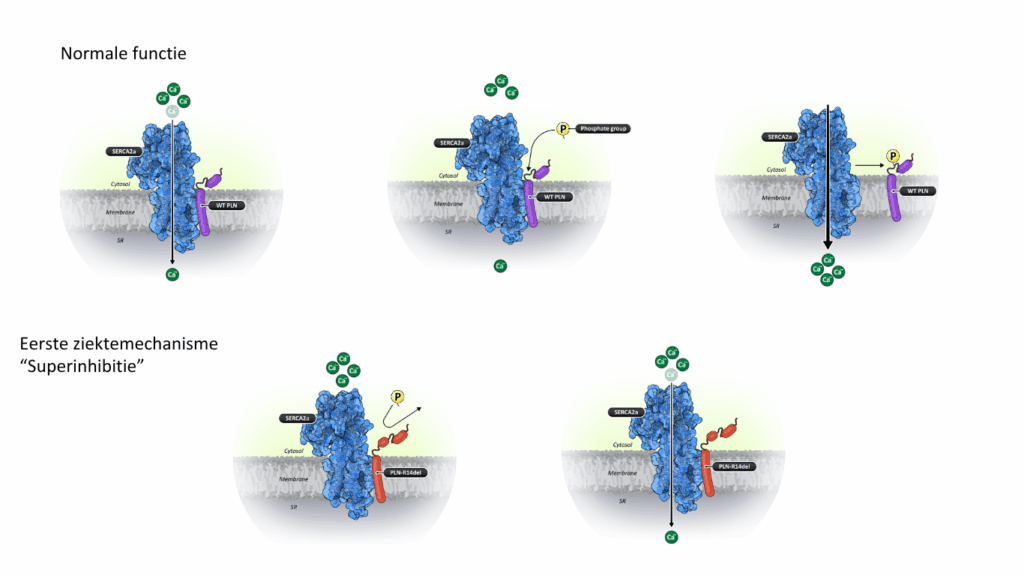
Tekst gaat verder onder afbeelding.
Zoals uitgelegd is PLN belangrijk bij het terugpompen van calcium in de hartcel. In het eerste onderzoek over PLN-R14del werd daarom ook direct gekeken wat PLN-R14del met calciumstromen doet. PLN-R14del bleek sterker te remmen op SERCA waardoor er minder calcium werd teruggepompt (een toename in functie van PLN dus). De theorie is dan snel rond: er is meer calcium in de hartcel en minder in de opslag.
De cel kan dus minder goed ontspannen en de volgende ronde minder krachtig samentrekken. Dit veroorzaakt hartfalen. Meer los calcium in de cel verhoogt ook de kans op ritmestoornissen. Het probleem is dat deze bevindingen niet helemaal teruggevonden worden in andere studies. Sommige onderzoeken vinden inderdaad dat PLN-R14del SERCA sterker remt. Andere onderzoeken vinden juist een zwakkere rem van SERCA (een afname in functie van PLN). Sommige studies vinden bijna geen veranderingen van de calciumstromen in het algemeen.
Theorie 2: PLN-R14del is een giftig eiwit
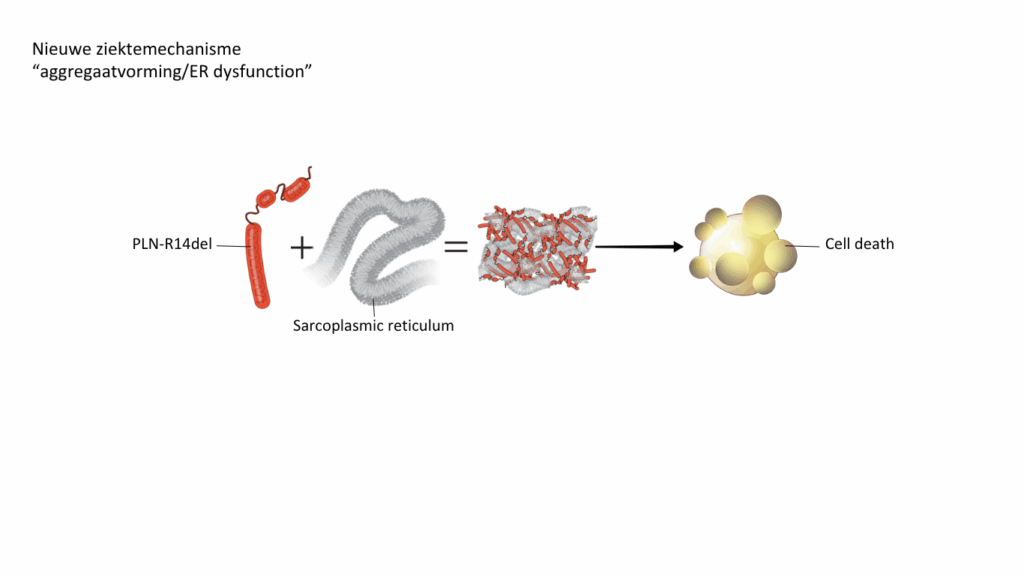
Tekst gaat verder onder de afbeelding.
De tweede theorie is dat het PLN-R14del eiwit zelf giftig wordt. Doordat er een klein stukje mist, verandert de vorm van PLN. In de cel zit een systeem dat controleert of eiwitten de goede vorm hebben. In PLN-R14del is dit systeem actiever. Ook vinden onderzoekers ophopingen van PLN eiwit in hartcellen. Deze ophopingen verstoren andere eiwitten en processen in de cel. Ze kunnen zelfs zo schadelijk zijn dat een hartcel erdoor dood gaat. De dode hartcellen kunnen niet vervangen worden door andere hartcellen.
In de plaats van dode hartcellen komt er littekenweefsel dat niet samen kan trekken en de geleiding van het hart verstoort. Ook deze processen kunnen hartfalen en ritmestoornissen veroorzaken. Het probleem bij deze theorie is dat er cellijnen en diermodellen zijn die wel een deel van de ziekte tonen, maar geen ophopingen van PLN eiwit vertonen.
Er is voor beide theorieën bewijs
Welke van de theorieën is waar? Of zijn beide waar? Feit is dat er bewijs is voor beide theorieën, die elkaar deels tegenspreken. Veel onderzoeken hebben gekeken naar het effect van PLN-R14del op calcium, maar soms vinden ze een toename, soms geen verandering en soms een afname in PLN activiteit. Op dezelfde manier worden niet in alle modellen ophopingen van PLN gevonden. Overigens is deze theorie ook extra lastig: als een cel inderdaad dood gaat door een ophoping is de cel daarna ook weg.
Deze tegenstrijdigheden geven aan hoe moeilijk het is om op dit detail een ziekte te begrijpen. Het laat ook zien hoe belangrijk het is de juiste cellen en dieren te gebruiken voor onderzoek. Onderzoek in nieuwe modellen zoals 3d modellen van menselijke hartcellen en het varkenshart geven hopelijk nieuwe aanwijzingen.
Hoewel het erg belangrijk is om te begrijpen hoe PLN-R14del ontstaat, is het niet noodzakelijk om de ziekte te kunnen behandelen. Veelbelovende behandelingen grijpen namelijk op het RNA of DNA niveau in (gentherapie). De oorzaak achter PLN nog een mysterie? Ja een beetje wel, maar geen obstakel voor een behandeling!