Met GIP (gentherapie informatiepakket) nemen we je mee in de wereld van gentherapie. De afgelopen jaren is er veel onderzoek naar gentherapie gedaan. Hierdoor is inzichtelijk geworden of en hoe gentherapie kan helpen met een behandeling voor PLN-R14del. Wij nemen je mee in de wereld van gentherapie. In deze derde les hebben we het over de risico’s en zorgen van gentherapie.
Overzicht gentherapie informatiepakket:
- Het gentherapie informatiepakket!
- GIP – Les 1: Cellen en het DNA
- GIP – Les 2: Mogelijke gentherapieën
- GIP – Les 3: Risico’s en zorgen
- GIP – Les 4: Bestaande gentherapieën
Zoals we eerder hebben gezien, bieden gentherapieën veel kansen om PLN te genezen. Tegelijkertijd hebben ook gentherapieën nadelen. In deze les staan we stil bij deze nadelen van gentherapie. Het is lastig om deze nadelen onder één noemer te vangen. Daarom worden de nadelen hier gesplitst. We staan eerst stil bij de nadelen van de verschillende therapieën en daarna bij nadelen van de toedieningsvormen.
Nadelen per therapie
Elke vorm van therapie die we hebben genoemd in de vorige les heeft zijn eigen voors en tegens. Onderzoek is dan ook nodig om helder te krijgen welke therapie de beste keuze is voor PLN.
Bij prime editing wordt de mutatie netjes hersteld, maar de benodigdheden voor prime editing passen niet in één virus. De kans dat er twee virussen in dezelfde cel terecht komen is kleiner dan de kans dat één virus in de cel komt. Hierdoor wordt in minder cellen het DNA hersteld of is een hogere dosering nodig waarbij ook meer bijwerkingen komen kijken. Daarnaast zijn er nog geen therapieën met prime editing op de markt en zou het proces om het op de markt te krijgen dus langer kunnen duren. Bij zowel prime editing als CRIPSR/Cas9 kunnen er per ongeluk andere plekjes in het DNA aangepast worden. Bij CRISPR/Cas9 is de kans hierop wel groter dan bij prime editing. Overigens wordt hier heel zorgvuldig op gescreend en is de kans klein dat zo’n verandering effect heeft.
Bij CRIPSR-Cas9 en het afvangen van PLN op RNA niveau vermindert de hoeveelheid PLN in een hartcel. De vraag is of mensen gezond kunnen leven met minder PLN. Het antwoord op deze vraag is niet bekend. Muizen kunnen wel met minder PLN (zie les 4), maar bij muizen is PLN waarschijnlijk minder belangrijk. Onderzoek zal dan ook moeten uitwijzen of mensen ook met minder PLN kunnen.
Het nadeel van algemene gentherapie zoals I-1C is dat ze de ziekte minder dicht bij de oorzaak aanpakken. Het voordeel is dat zo’n therapie voor meer patiënten geschikt is en daarnaast ook goedkoper uit kan vallen omdat ze aan grotere groep patiënten gegeven kan worden.
Nadelen van AAVs
Ook de toedieningsvorm van de therapie kan nadelen hebben. We staan hier vooral stil bij de twee belangrijkste nadelen van AAVs. Als eerste is een AAV een virus net zoals een verkoudheidsvirus. Dit betekent dat je immuunsysteem er antilichamen tegen kan maken (ook al veroorzaakt een AAV dus geen ziekte). Als je deze antilichamen aan het begin van de therapie al hebt, zal de therapie niet werken. Gelukkig zijn hier oplossingen voor zoals onderdrukking van het immuunsysteem en het technisch verbeteren van AAV’s. Als je nog geen antilichamen hebt aan het begin van de therapie, kun je antilichamen ontwikkelen waardoor slechts eenmalige toediening mogelijk is. Dit laatste is overigens niet per se een probleem omdat er bij gene editing in principe slechts één behandeling nodig is. Een tweede nadeel is dat een te hoge dosis AAVs slecht is voor je lever. Er wordt dan ook gestreefd naar een balans tussen zoveel mogelijk AAVs zodat je zoveel mogelijk hartcellen kan behandelen en zo min mogelijk AAVs zodat je lever er niet onder lijdt.
Toediening
Er zijn eigenlijk twee mogelijkheden voor de toediening van gentherapie. De therapie kan toegediend worden door injectie het hart. De procedure hiervan is vergelijkbaar met hartkatheterisatie. Hoewel dit ingrijpender is dan een pilletje innemen, is het eenmalig. Deze therapie zou waarschijnlijk voor gene editing gelden en wordt ook voor I-1c gebruikt. De toediening van een therapie die het PLN RNA niveau naar beneden brengt, is anders. Deze behandeling kan gewoon in een ader geïnjecteerd worden. Hiervoor zijn echter wel vaak herhaalde doseringen nodig (bijvoorbeeld elke maand).
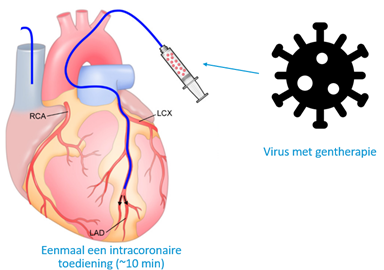
Figuur 1 Toediening van virus met gentherapie via injectie in het hart.
Zorgen
Er kunnen ook andere vragen leven over gentherapie. Tast het je genoom of je persoon aan? En wat zijn de gevolgen voor nageslacht? Om bij het eerste te beginnen, alleen gene editing verandert iets in je genoom. Een behandeling die ingrijpt op het RNA verandert het DNA niet. Voor gene editing gelden strikte controles dat alleen het PLN gen wordt gecorrigeerd zonder ongewenste veranderingen. Gentherapie gericht op PLN zal geen gevolgen hebben op wie je verder bent.
Genetische therapieën worden niet doorgegeven aan het nageslacht. Gentherapie zit namelijk in een specifiek jasje dat alleen door hartcellen opgenomen kan worden. Daarnaast zit er een soort slot op het gen waarvan de sleutel alleen in hartcellen aanwezig is. Hierdoor zal het gen bijna tot helemaal niet in andere cellen dan het hart tot uiting komen.
De lange termijn gevolgen van gentherapie zijn niet bekend en zullen pas in de loop van jaren bekend worden (lange termijn betekent hier meer dan 5 jaar). In onderzoek naar een behandeling zal vooral gekeken worden naar het effect op korte termijn en over de loop van een aantal jaar. Langere opvolging van patiënten zal wel plaatsvinden, maar valt buiten het onderzoek dat noodzakelijk is om gentherapie op de markt te brengen.
Een andere zorg is de prijs. Een gentherapie voor een zeldzame ziekte kan ontzettend duur zijn. Voor bestaande gentherapieën lopen de kosten op van meerdere tonnen tot 1 miljoen per behandeling. Stichting PLN zet zich daarom niet alleen in voor een behandeling maar ook voor een betaalbare behandeling.
Onderzoek moet nog uitwijzen in welke stadium van de ziekte je het beste behandeld kan worden. In principe geldt: hoe eerder de behandeling, hoe minder de ziekte het hart aangetast zal hebben. Waarschijnlijk zullen de eerste menselijke onderzoeken gedaan worden op patiënten die zich in en vergevorderd stadium bevinden omdat dat ethisch beter te verantwoorden is.
Het is duidelijk dat gentherapie veelbelovend is voor PLN, maar ook nadelen kent. Komende jaren zullen we zien welke therapie het beste werkt en naar klinisch onderzoek mag om patiënten te behandelen. In de volgende les kijken we welke gentherapieën er op dit moment voor PLN ontwikkeld worden.
