Met GIP (gentherapie informatiepakket) nemen we je mee in de wereld van gentherapie. De afgelopen jaren is er veel onderzoek naar gentherapie gedaan. Hierdoor is inzichtelijk geworden of en hoe gentherapie kan helpen met een behandeling voor PLN-R14del. Wij nemen je mee in de wereld van gentherapie. In deze tweede les vertellen we meer over de verschillende soorten gentherapie en de mogelijkheden hiervan.
Overzicht gentherapie informatiepakket:
- Het gentherapie informatiepakket!
- GIP – Les 1: Cellen en het DNA
- GIP – Les 2: Mogelijke gentherapieën
- GIP – Les 3: Risico’s en zorgen
- GIP – Les 4: Bestaande gentherapieën
In de vorige les hebben we gezien dat elke cel een kern bevat met daarin een soort kookboek voor de cel, het DNA. Dit DNA bevat genen (recepten) die vertaald worden in RNA (boodschappenbriefjes) zodat een eiwit (gerecht) samengesteld kan worden. Verder hebben we gezien dat gentherapie de meeste potentie heeft om PLN te genezen. In deze les staan we stil bij verschillende soorten van gentherapie.
Er zijn verschillende soorten gentherapie. Hierbij is het belangrijk om onderscheid te maken dus gentherapie in het algemeen of gene editing waarbij het DNA wordt aangepast. Gentherapie in het algemeen werkt op RNA niveau: er wordt een extra gen ingebracht of een gen weggevangen. Voor PLN zijn er drie soorten behandelingen mogelijk (Figuur 1): (1) gene editing; (2) het foute boodschappenbriefje, het foute RNA wegvangen; (3) algemene gentherapie die ook voor andere hartziektes zou kunnen werken.
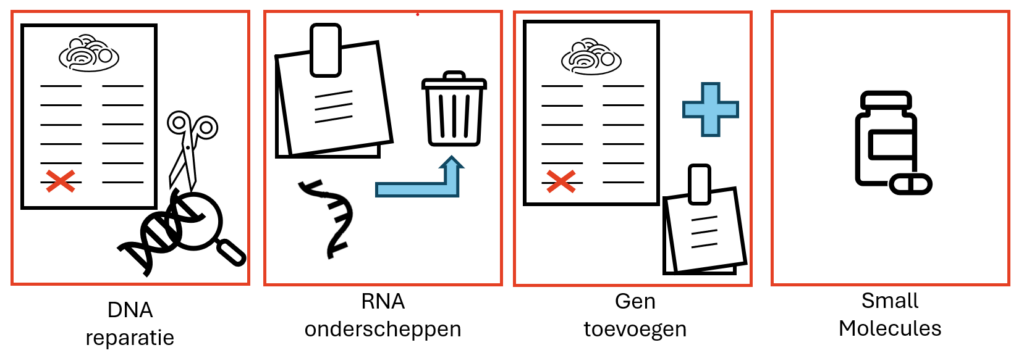
Figuur 1 Drie soorten gentherapie voor PLN R14del. In optie 1 wordt het DNA gerepareerd zodat de fout verdwenen is. In optie 2 wordt het verkeerde RNA verwijderd zodat er minder kapot eiwit wordt gemaakt. Ten slotte wordt bij optie 3 een gen (dat kan een gezond PLN gen zijn, maar ook een ander gen dat het hart helpt) toegevoegd.
In deze les staan we eerst stil bij gene editing, vervolgens bij gentherapie op RNA niveau en ten slotte bij de manier waarop gentherapie wordt toegediend. In volgende lessen komen de voor- en nadelen van gentherapie en verschillende gentherapieën die al in patiënten gebruikt worden aan het bod.
Gene editing
Een bekende vorm van gentherapie is CRISPR/Cas9. Deze techniek is eigenlijk afgeleid van de natuur en komt uit bacteriën. De deletie van een heel aminozuur kan met CRISPR/Cas9 niet hersteld worden. Wel kan het foute gen helemaal kapot gemaakt worden zodat er geen fout eiwit meer wordt gemaakt. Eigenlijk wordt het foute recept weggegooid zodat er ook geen fout gerecht meer wordt gemaakt. Een andere vorm van gentherapie is prime editing waarbij de verandering in het DNA hersteld kan worden. CRISPR/Cas9 en prime editing lijken erg op elkaar. In feite moeten er drie dingen gebeuren: als eerste moet de plek met de verandering op worden gespoord in het hele genoom, als tweede wordt het DNA geknipt en ten slotte moet de fout worden hersteld (Figuur 2). Hieronder werken we deze stappen uit met aandacht voor de verschillen tussen CRISPR/Cas9 en prime editing:
- Het opsporen van de fout is makkelijker gezegd dan gedaan. Ons DNA bestaat namelijk uit zo’n 3.000.000.000 letters! Maar met een stukje gids RNA van 17-24 letters is het mogelijk om heel precies de locatie met de mutatie op te sporen;
- De tweede stap verschilt tussen CRISPR/Cas9 en prime editing. CRISPR/Cas9 bindt aan het DNA en maakt een breuk in beide strengen van het DNA, terwijl er bij prime editing slechts één streng van het DNA verbroken wordt. Vergelijk het met een ladder waarvan de zijkant wordt doorgezaagd; aan één kant of aan beide kanten. Je kunt je voorstellen dat de tweede manier veel makkelijker is;
- Ten slotte moet de breuk in het DNA hersteld worden. Bij CRISPR/Cas9 moet de cel dit zelf doen. Doordat er een breuk in beide DNA strengen zit, zullen er foutjes ontstaan bij het herstellen van de breuk (er raken een paar stukjes van het verscheurde recept kwijt). Het gevolg zal waarschijnlijk zijn dat het gen helemaal kapot is. Dit klinkt niet als een oplossing, maar kan wel degelijk goed zijn. Soms is geen recept namelijk beter dan een slecht recept.
Bij prime editing daarentegen wordt er een eiwit meegestuurd dat de fout in het DNA aan de hand van een meegeleverd sjabloon herstelt. Er komt als het ware een nieuw tijdelijk recept met daarop het missende ingrediënt (het aminozuur arginine op de 14e positie) zodat dit overgeschreven kan worden in het echte recept (het DNA). Met prime editing kun je dus heel nauwkeurig allerlei soorten fouten herstellen in het DNA. Het grote voordeel is dat hiermee de verandering helemaal bij de wortel kan worden aangepakt.
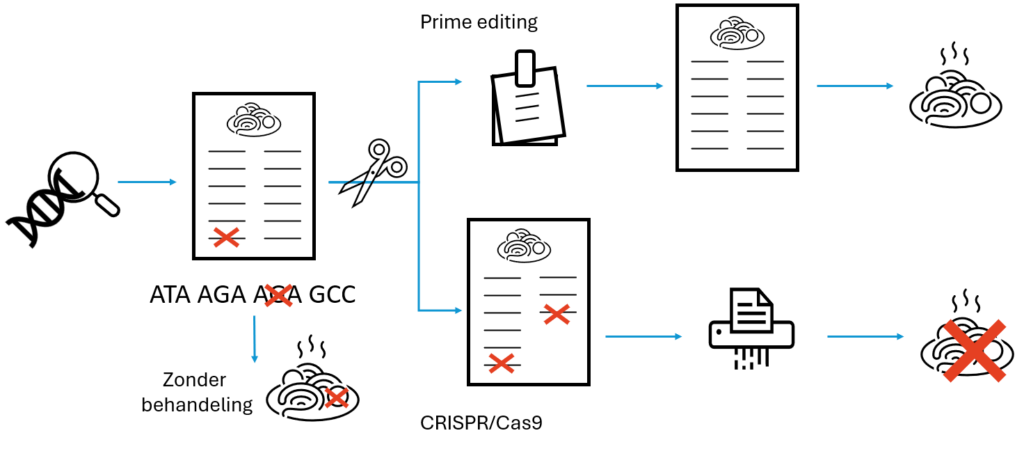
Figuur 2 Het mechanisme achter prime editing en CRISPR/Cas9. Zonder behandeling wordt er van het gemuteerde PLN gen een verkeerd boodschappenbriefje en dus een verkeerd gerecht gemaakt. Bij prime editing wordt er een breuk in het DNA gemaakt en daarna wordt met een sjabloon het gen herschreven. Hierdoor wordt het boodschappenbriefje en recept weer goed. Bij CRISPR/Cas9 wordt het gemuteerde gen juist kapot gemaakt. Het boodschappenbriefje gaat hierdoor ook kapot en wordt vernietigd. Het verkeerde recept wordt dan dus ook niet meer gemaakt.
Gentherapie op RNA niveau
Naast gene editing zijn er ook verschillende andere vormen van gentherapie die een mogelijke behandeling voor PLN zijn. Naast algemene vormen van gentherapie is dit het wegvangen van verkeerd PLN RNA. Zoals gezegd kun je een verkeerd gen vergelijken met een verkeerd recept dat resulteert in een verkeerd boodschappenbriefje en dus een verkeerd gerecht. Stel dat twee koks samen een grote pan soep maken. Ze hebben beide een kopie van het recept, maar één kopie bevat een foutje. De kok met het foute recept zal het verkeerde boodschappenlijstje maken en daardoor de hele soep laten mislukken. Terug naar het DNA kun je het probleem oplossen door het foute RNA af te breken. Dit kun je op verschillende manieren bereiken. Al deze manieren hebben gemeenschappelijk dat er iets aan het RNA wordt gehangen waardoor het naar de afvalverwerking gaat.
Ten slotte zijn er nog algemene vormen van gentherapie. We noemen er hier twee. De eerste sluit eigenlijk aan bij het wegvangen van het RNA. Bij deze behandeling wordt er extra gezond PLN gen ingebracht. In plaats van het wegvangen van het kapotte boodschappenbriefje, zorg je dat er meer van het goede boodschappenbriefje komt. De tweede optie is I-1c, een behandeling die nu in patiënten wordt getest. Deze behandeling grijpt aan op een eiwit dat aan PLN bindt en de structuur van PLN beïnvloedt. Hierdoor wordt de activiteit van PLN geremd. Beide behandelingen zouden ook voor hartziektes die niet door PLN veroorzaakt worden gebruikt kunnen worden, omdat PLN ook in andere hartziektes slechter werkt.
Vervoer
Een van de grote uitdagingen bij gentherapie is om de therapie in de cel te krijgen. Bij een ‘normaal’ medicijn, meestal een klein molecuul, dringt het medicijn zelf de cel binnen. Gentherapie echter kun je niet in een pilletje stoppen, het moet toegediend worden met een injectie. Als je de therapie zonder verpakking in het bloed toedient, zal het snel afgebroken worden en geen effect hebben. Daarom moet het verpakt worden. Er zijn twee soorten verpakkingen die veel onderzocht worden. Dat zijn virussen en vetbolletjes (lipid nano particles).
- Een virus is een envelop met daarin RNA of DNA. Een virus dringt een cel binnen, maakt nieuw RNA of DNA en verspreidt zich zo. We kunnen een virus ook zo aanpassen dat het niet zijn eigen vracht, maar een stukje genetisch materiaal dat wij willen in een cel brengt. Als het over virussen voor gentherapie gaat, gaat het eigenlijk altijd over AAV’s. AAV’s hebben namelijk belangrijke voordelen: (1) er zijn verschillende types die verschillende weefsels kunnen binnendringen; (2) AAV’s kunnen het DNA niet aanpassen en veroorzaken daar dus geen bijwerkingen; (3) AAV’s zijn wel virussen maar veroorzaken geen ziekte (zoals een griepvirus wel doet);
- Vetbolletjes kunnen in het lab gemaakt worden en zo aangepast worden dat ze doen wat we willen. In dit geval kunnen dus de benodigdheden voor gene editing of het RNA voor een andere gentherapie in een vetbolletje gestopt worden. Het vetbolletje kan vervolgens zo worden aangepast dat het vooral hartcellen binnendringt. Op dit moment is het echter nog lastig om specifiek het hart te behandelen.
Naast deze behandelingen zijn er ook andere manieren om gentherapie in een cel te krijgen zoals koppeling aan een antilichaam of eiwit. Stichting PLN werkt samen met verschillende bedrijven die dit onderzoeken. Hierdoor blijven alle opties open, ook als een van de vervoersopties niet blijkt te werken.
Uit deze les is duidelijk geworden dat er binnen gentherapie verschillende mogelijke behandelingen zijn. Tegelijk hebben die behandelingen wel nadelen. De volgende les staan we stil bij deze nadelen.
